みなさん、こんにちは!
科学コミュニケーターの沈晨晨(しぇん ちぇんちぇん)です。
未来館恒例のノーベル賞予想の季節になりました。
私は初参加ながら、自信をもってノーベル生理学・医学賞を予想させていただきます!
私の予想は、このお二人の共同受賞です!

Photo by Gerbil via Wikimedia Commons, CC BY-SA 3.0 (リンクは削除されました)

写真提供 静岡県立大学
なぜこのお二人かというと、がん治療の新しい道を切り拓いたからです!
免疫(病原体やがん細胞を攻撃して体を病気から守るしくみ)でがんを治すという研究です。
ただし、従来の免疫治療とは発想が違います。
はじまりは1995年、アリソン博士のある発見でした。
その当時は免疫を活性化させる分子に注目が集まり、さまざまな病気の治療薬が期待されていました。
しかし、彼の発見はその逆で、免疫の働きを抑える分子だったのです。
当時のほかの研究者にとっては考えられない、聞きたくもないようなものでした。
でも、これが免疫治療のブレイクスルーとなります。
アリソン博士の狙いは、免疫システムのブレーキを解除することでがん細胞への攻撃を行わせることにあったのです(ここが革新的!)。
アリソン博士は長年の研究成果を認められ、ガードナー国際賞を2014年に受賞。
さらに今年2015年はラスカー賞の臨床部門に輝きました。
ガードナー国際賞もラスカー賞も、ノーベル賞の前哨戦などといわれる賞です。
そして、本庶博士は別の抑制分子を発見し、東洋のノーベル賞とも言われる唐奨(唐賞)を2014年にアリソン博士と共同受賞しています。
いったいどんな研究なのか気になりますよね?
これから、以下の流れで免疫の基本的な知識からもう少し詳しく紹介したいと思います。
I. 免疫ってなに?
II. 免疫細胞の働きを抑えるシステムってなに?
III. 新しい免疫治療ってなに?
I. 免疫ってなに?
免疫は細菌やウイルスなどの病原体やがん細胞を認識して破壊し、体の健康を守るしくみです。
主役は免疫細胞で、ほとんどがいわゆる白血球です。
相手の性質と強さによって、登場する免疫細胞の種類と戦略が違います(かしこいですね)。
免疫細胞にとっては、細菌やウイルスなど外部からの病原体だけでなく、自分の体の死んでしまった細胞の残骸やがん化した細胞なども攻撃する相手です。
守るべき自分の細胞と、攻撃相手とを見分ける目印となるのは、それぞれがもつタンパク質で、これを抗原と呼びます。
最初に登場する免疫細胞はマクロファージなどの食細胞です。
自分の健康な細胞以外、相手かまわずなんでもパクパク食べます。
ここまでの反応は「自然免疫」と言います。
でも、この自然免疫で処理できなければ、「獲得免疫」というもっと高いレベルの反応がはじまります。
特定した相手のみに反応するので、ピンポイントで相手を攻撃するのに効果的です。
獲得免疫が発動するには、まず免疫反応での司令官となるヘルパーT細胞という重要な細胞を活性化しなければなりません。
活性化したヘルパーT細胞はキラーT細胞やB細胞などたくさんの種類の免疫細胞に抗原と戦う命令を出して、免疫細胞の戦闘力をさらに高めます。
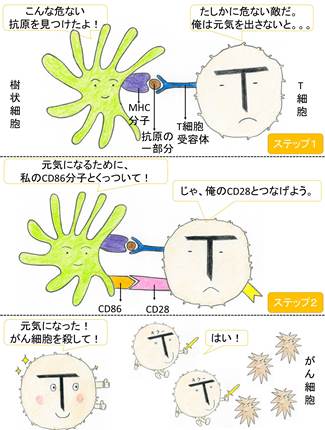
T細胞の活性化には2つのステップがあります。(図1)
1. マクロファージやその仲間の樹状細胞などが抗原の一部分をもって、T細胞にくっつく。
2. 樹状細胞などの表面にあるCD80やCD86という補助刺激分子が、T細胞の表面にあるCD28という補助刺激分子としっかりくっつく。 (ほかの補助刺激分子もありますが、ここでは重要なものだけを紹介します)
抗原の一部分を、ヘルパーT細胞に掲げることで、これが攻撃すべき敵であることを認識できるようになるのです。
このようにしてT細胞を活性化することが、がん細胞を攻撃する最初の一歩となります。
活性化できれば、ナチュラルキラー細胞やキラーT細胞などが、がん細胞を攻撃しはじめます。
活性化したT細胞はがん細胞の天敵であるキラーT細胞などに
がんに攻撃する命令を出したり、攻撃力を高めたりします。
ここで疑問が出てきますね。
免疫細胞はがん細胞を攻撃できるのに、なぜがんが発症するのでしょうか?
この理由は次で説明します。
II. 免疫細胞の働きを抑えるシステムってなに?
アリソン博士と本庶博士の発見によって、T細胞の活性化を抑えるシステムがわかりました。
がん細胞は、その抑制システムを利用して、免疫細胞の攻撃から逃れているのです(ずるいですね)。
うまく逃れたがん細胞がどんどん増殖すると、病気レベルのがんになってしまいます。
では、なぜ抑制システムが存在しているのでしょうか?
免疫細胞はとても優秀で、健康な細胞を攻撃しないようにしながら抗原と戦っていますが、 たまに暴走して健康な細胞も攻撃してしまうことがあります。
この行き過ぎた反応を防ぐために、免疫細胞を抑えることが必要なのです。
アリソン博士と本庶博士は、T細胞の活性化を抑えるシステムに役立っている分子をそれぞれ別々に発見しました。
アリソン博士は1995年にCTLA-4分子を初めて発見しました。
本庶博士は1992年にPD-1分子の遺伝子を見つけ、1998年にはPD-1分子が実際にT細胞の興奮を抑えることを明らかにしました。
CTLA-4 とPD-1では抑制のしくみがまったく違います。
CTLA-4による抑制のしくみ(図2)
T細胞を活性化するステップが2つあります。(図1を参考にしてください)
ステップ2では樹状細胞などのCD80やCD86という分子がT細胞のCD28とくっつきます。
でも、T細胞はCD28だけでなく、CTLA-4という分子を表面に出すことがあります。
この分子は、樹状細胞などのCD80やCD86と結合できるのです。
むしろ、CTLA-4のほうがよくくっつきます。
CD28の代わりにCTLA-4という分子とくっついたら、T細胞のCD28と結合することができなくなり、T細胞の活性化もできなくなります。
つまり、T細胞を活性化する過程をじゃましているわけです。
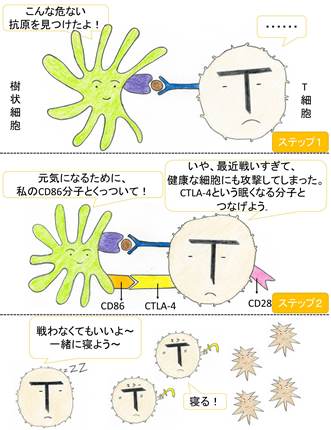
T細胞の活性化が抑制されて、がんへの攻撃力が弱くなります。
PD-1による抑制のしくみ(図3)
PD-1分子はT細胞を活性化する過程のじゃまはしませんが、活性化したT細胞を抑える働きをします。
活性化したT細胞はIFN-γというタンパク質を出します。
ほかの自分の細胞がIFN-γを浴びると、その細胞の表面にPD-L1分子が現れます。
PD-1分子とPD-L1分子がくっつくことで、T細胞は攻撃をやめます。
がん細胞のずるいところは、このPD-L1分子を健康な細胞と同じように表面に付けるところです。
これによって健康な細胞のふりをして、活性化T細胞から逃げようとするんですね。
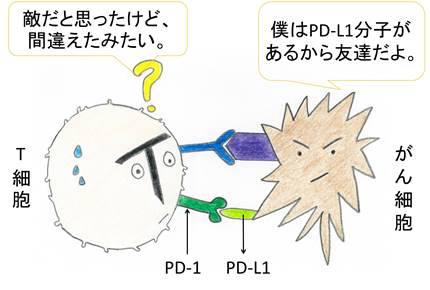
ところが、がん細胞上のPD-L1分子とPD-1分子が結合すると、
T細胞の攻撃が抑制されます。
III. 新しい免疫治療ってなに?
CD80やCD86がCTLA-4と結合するのを阻害して、T細胞の不活性化を防ぐ方法です。(図4)
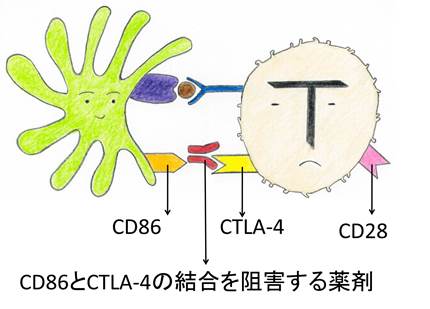
結合相手を失ったCD80やCD86は、
T細胞のCD28と結合するようになるはずです。
CD28と結合すれば、T細胞は活性化するのでしたよね。
T細胞が活性化すれば、がん細胞への攻撃が始まるはずです。
アリソン博士が1995年頃にこの考えを初めて公開したとき、多くの研究者たちは信じませんでした。
それでもアリソン博士はあきらめずに、約15年の臨床試験を経て、イピリムマブという薬剤を開発しました。
CD80やCD86とCTLA-4の結合を阻害するような薬です。
そして、2011年に皮膚がんの一種である悪性黒色腫(メラノーマ)の治療薬としてアメリカ食品医薬品局に承認されました。
治療効果として患者さんの2割は生存期間が4年以上であり、10年を超える患者さんもいます。
アリソン博士の臨床試験の結果から見ると、短期的な治療効果は著しくないですが、患者さんの生存期間はほかのどの治療法よりも長くなりました。
また、1種類のがんだけでなく、たくさんの種類のがんに効果的です(この点もすごく評価されています)。
アリソン博士が切り拓いた、新しい免疫療法はどんどん注目されています。
次にPD-1分子とPD-L1分子の結合を阻害する薬剤が開発されました。(図5)
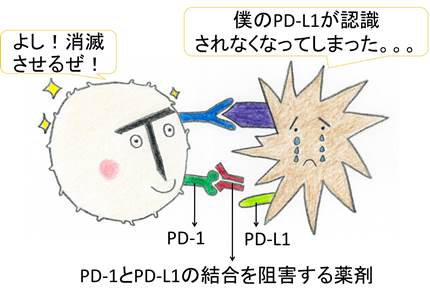
活性化したままのT細胞は、がん細胞を攻撃します。
CTLA-4に負けないほど効果的です。
それが、ペンブロリズマブとニボルマブ。
メラノーマの治療薬として、2014年にアメリカ食品医薬品局に承認されました。
日本では2014年7月にニボルマブが承認され、2014年9月に小野薬品工業から発売されています。
最近のアリソン博士の論文では、CTLA-4とPD-1でのT細胞の抑制方法が異なることを利用し、抗CTLA-4治療と抗PD-1/PD-L1治療を組み合わせれば、もっと効果的にがんを治療できると示されています。
また、CTLA-4やPD-1と似ているほかの分子をどんどん見つけて、新しい薬剤の開発をしています。
さらに、手術、放射線治療、がんワクチン治療などと組み合わせる開発も期待できます。
アリソン博士と本庶博士はがんの免疫治療に大きな貢献をしました。
免疫の攻撃からまんまと逃げようとするがん細胞。
それに対して、免疫にブレーキをかけている要因を抑えることで、免疫細胞が十分に活躍できるようにして、自分の免疫の力でがんを治すという新しい道を切り拓きました。
いつか、がんも普通の風邪のように治せるようになるかもしれません。
その第一歩を築いたお二人が、今年のノーベル生理学・医学賞を手にするのではないでしょうか。
皆さまも以下のサイトから予想に参加してください!
ノーベル賞を予想しよう!2015(現在は公開を終了)
2015年ノーベル賞を予想する
生理学・医学賞①免疫制御の分子の発見とがん治療への応用 (リンクは削除されました)
生理学・医学賞②細胞の中のお掃除係 (リンクは削除されました)
生理学・医学賞③ゲノムを編集するツールCRISPR/Cas9の開発 (リンクは削除されました)
生理学・医学賞④ Coming Soon!
物理学賞①電気を通す絶縁体!? (リンクは削除されました)
物理学賞②あったぞ!太陽系外惑星 (リンクは削除されました)
物理学賞③ Coming Soon!
化学賞①モバイル機器の原動力を開発した男たち
化学賞②小さな孔から大きな世界へ (リンクは削除されました)
化学賞③縁の下の力持ちDNAマイクロアレイ (リンクは削除されました)
化学賞そのほか Coming Soon!
今年もその瞬間をニコニコ生放送で中継します。
ノーベル賞発表の瞬間をみんなで迎えよう (リンクは削除されました)







