こんにちは!科学コミュニケーターの石田です。
浜口の予想に引き続き、生理学・医学賞の予想、第2弾!
私の予想は、細胞を光で操作する方法を確立し、神経科学を変えたこちらの三人です!!!
オプトジェネティクス(光遺伝学)の確立に対する貢献

(左)
ピーター・ヘーゲマン(Peter Hegemann)博士 1954年生まれ
ドイツ フンボルト大学
写真提供:Peter Hegemann博士
(真ん中)
カール・ダイセロス(Karl Deisseroth)博士 1971年生まれ
アメリカ スタンフォード大学
写真提供:Karl Deisseroth博士
(右)
エドワード・ボイデン(Edward Boyden)博士 1979年生まれ
アメリカ マサチューセッツ工科大学
写真提供:Edward Boyden博士
オプトジェネティクスとは?
必殺技みたいでかっこいいという理由でつけた名前ではありません!
オプトジェネティクス(optogenetics)はopto(光)とgenetics(遺伝学)を合わせた造語です。特定の色の光に反応する光感受性タンパク質オプシン(opsin)を神経細胞に遺伝子導入することで、その生物の神経細胞のはたらきを、光のオンオフで自由に操作できるようにする技術です。
なぜ必要?
脳科学者や神経科学者には「人間の行動がどのような神経活動によってコントロールされているのかを知りたい」という夢があります。(もちろん私も知りたい...)
そのためには、「観察」が重要ですが、「操作」もできるようになれば仮説を確かめることできるようになります。
脳科学や神経科学の分野で、まず、飛躍的に向上してきたのが観察技術です。科学者たちはある行動をしているときに、どの神経細胞がどう活動しているのかをひたすら観察してきました。しかし、いくら観察を極めても神経活動が分かったとは言い切れないのです。
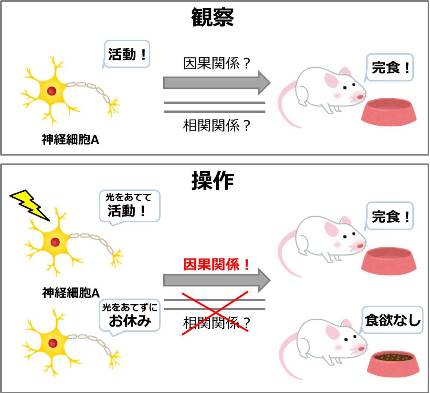
例えばマウスの神経細胞Aが活動するときにもりもりごはんを食べることを観察できたとします。でも、それだけでは神経細胞Aの活動とごはんをもりもり食べることが相関しているだけなのか、神経細胞Aが活動したからもりもりごはんを食べるようになったのか(因果関係なのか)は分からないのです。
そこで必要なのが「操作」です。神経細胞Aの活動を増やしたり止めたりしたときの行動を見ることで、神経細胞Aの活動がもりもりごはんを食べることの本当の原因なのかがわかるのです。
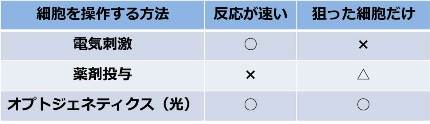
これまでも神経細胞を操作する技術として、電気刺激や薬剤投与が使われてきました。しかし、電気刺激は神経活動をミリ秒単位で操作できる一方で、電極の周りのターゲットではない細胞にまで影響を及ぼしてしまうという問題があります。薬物投与は、ある程度狙いを定めて神経細胞を操作できますが、ミリ秒単位では操作できません。そんななか、操作研究に光をもたらしたのがオプトジェネティクスなのです! オプトジェネティクスは光だけにミリ秒単位で、かつ狙いを定めて神経細胞を操作することができるのです。
このようにいいとこ取りのオプトジェネティクス。どのような技術なのでしょうか?
オプトジェネティクスを生み出した技術
チャネルロドプシンの発見
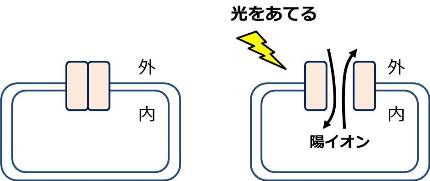
光合成をする微生物のクラミドモナスから、光を当てると形が変わる膜タンパク質をドイツのヘーゲマン博士が発見しました。変形することで陽イオン(H+、Na+、K+)が細胞の内側から外側へ流出、あるいは逆方向の流入が起きるようになります。こうした膜タンパク質はチャネルロドプシンと総称されるようになりました。チャネルは運河の意味で、ロドプシンは人間の網膜にもある光に反応するタンパク質のことです。
チャネルロドプシンを神経細胞に発現させるというアイデア
このチャネルロドプシンを神経細胞に発現させれば、神経細胞をコントロールできるのではないかと考えたのがアメリカのダイセロス博士とボイデン博士です。
このアイデアを理解するために、まず神経細胞のお話をしましょう。
刺激が加わった神経細胞は、活性化して「活動」します。この「活動」とは、具体的に何が起きているのでしょうか?
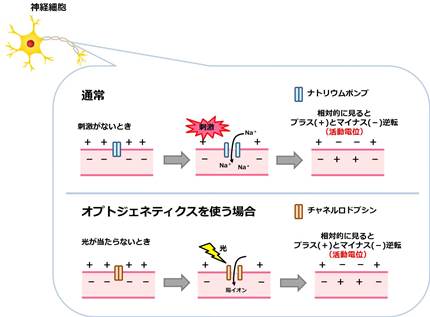
何も刺激を受けていない状態では神経細胞の内側はマイナス(-)、外側はプラス(+)に保たれています。そこに、刺激が加わるとNa+イオンチャネルが開き、Na+が細胞内に流れ込みます。すると、相対的に見て神経細胞の内側がプラス(+)、外側が(-)となり細胞膜での電位が逆転します(活動電位と呼びます)。この電位の逆転状態が神経細胞の長い突起を波のように伝わっていき、末端で隣の神経細胞に情報を伝えます。これを神経細胞の活動と呼んでいます。
オプトジェネティクスでは、遺伝子操作を使って神経細胞にチャネルロドプシンを発現させます。光が当たると、チャネルロドプシンが開いて、陽イオンを通すようになります。すると、陽イオンが細胞内に流れ込み、膜電位が逆転し、神経細胞の活動が起こるのです。
このような技術により、光のオンオフで狙った神経細胞のはたらきをすばやく操ることができるようになったのです。では、実際にオプトジェネティクスによってこれまでどのようなことが明らかになったのでしょうか?そして、どのような応用が期待されるのでしょうか?
オプトジェネティクスによる成果例
さまざまな神経細胞の働きを明らかにする
オプトジェネティクスを用いて、標的となる神経細胞 をオンオフさせ行動の違いを見ることで、たとえば、セロトニンという物質を分泌する神経細胞が我慢強さに関わっていることや脳のある特定の部位が「やる気スイッチ」であることがマウスでわかりました(マウスでは脳の腹外側線条体という部位にある「ドーパミン受容体2型陽性中型有棘ニューロン」という特定の神経細胞がそのスイッチでした)。
記憶へのアプローチ
オプトジェネティクスを用いて、うつ状態になったマウスの楽しかった記憶を人為的に活性化させることでうつ状態を改善できたり、ある記憶に対応する細胞の集まりを活性化させることで記憶をよみがえらせたりすることが報告されています。
fMRIなどの脳の観察技術の精度向上
オプトジェネティクスとfMRIを組み合わせることで特定の神経細胞の活動がfMRIの信号にどのような変化をもたらすのか、つまり全脳の活動にどのような影響を与えるのか調べることができます。人にオプトジェネティクス実験をすることはできませんが、マウス実験で得たオプトジェネティクスのデータとfMRIのデータを付き合わせることはできます。それを使えば、人間のfMRIデータからもっと多くのことを推測できるようになると期待されます。
※DBS(Deep Brain Stimulation)
脳の特定の部位に電気刺激を送る方法。電極を脳深部のターゲットに挿入し、この電極とケーブルでつながった装置を患者の胸の皮膚の下に埋め込む。パーキンソン病の治療法として25年以上の歴史があり世界中で13万人以上の患者さんが受けている。 2015年オプトジェネティクスで得られた知識をもとにマウスへのDBSの方法を改良したところ、オプトジェネティクスと同等の治療効果が得られた ことが報告されている。
このようにオプトジェネティクスで神経活動の理解が深まることで、神経細胞をターゲットとした治療の幅が広がるかもしれません。人の健康を維持するためにどこまで脳や神経細胞に手を加えるのか...議論される日も近いことでしょう。何より、私たちがふだん当たり前のように行っている「思考活動」のことが、オプトジェネティクスのおかげで急速にわかり始めているのです。
私たちの常識やこれからの生活に衝撃を与えうる技術であるオプトジェネティクス。この技術こそ、ノーベル賞を受賞するのではないでしょうか?
【取材協力】慶應義塾大学 医学部 精神・神経科学教室 田中謙二准教授
【参考文献】 羊土社 「実験医学2015 12月号 特集オプトジェネティクス」
2017年ノーベル賞を予想する
生理学・医学賞① コレステロール低下薬 スタチンの発見
生理学・医学賞② 神経科学を変えた!オプトジェネティクス(この記事)







