こんにちは。科学コミュニケーターの鈴木啓子です。
いよいよこの季節がやってきました!ノーベル賞です!毎年私は新聞を楽しみにしていました。今年のノーベル賞は何かな、おっ意外なのがきたな、なんて。……でも、今年は予想する側に!
当たるかどうかハラハラですが、これから私が予想した生理学医学賞の受賞者を発表します!
鈴木啓子の予想する生理学医学賞
受賞者: Douglas Coleman (カナダ) 写真左
Jeffrey M. Friedman (米国) 写真右
受賞テーマ: レプチンの発見とその作用機序の解明

この研究のここがスゴイ!
みなさん、食事の前はおなかがすいていますよね? そして、そしてご飯を食べて満腹になると、それ以上は食べたくなくなるはずです。このとき、体の中で「レプチン」という食欲を押さえるホルモンが働いています。もしもレプチンが働かなければ、際限なくご飯を食べてしまいます。それを繰り返すと太ってしまいますね……!
Colemanさんはレプチンを発見した人、Friedmanさんはレプチンがどんな風に体の中で働いているのかを解明した人です。この研究のおかげで、健康ならば体重はほぼ一定に保たれているメカニズムを知ることができました。
さて、レプチンはいつ頃、どこから分泌されるのでしょうか。ご飯を食べてエネルギーが蓄積されると脂肪細胞からレプチンが分泌されます。何よりすごいのは、レプチンは血液中を流れていって、脳に直接働きかけるのです!その場所は脳の視床下部。視床下部と一部の脳領域には、脳と血管の間にある強いバリアがありません。だから、レプチンは視床下部に直接働きかけることができます。
レプチンが視床下部に届くと、脳は「エネルギーがたまってきた=おなかいっぱいになった」という信号をもらったぞ、と判断して、「もうこれ以上食べないように」という命令を出します。そうするとレプチンの分泌が止まります。こんな風に、レプチンは自己点検をして、自分の分泌量を調節しています。このやり方をフィードバックと呼びます。
満腹因子(レプチン)の発見
さて、前述の通り、Colemanさんがレプチンを発見しました。といっても、レプチンという名前は後からついて、Colemanさんは「満腹因子」と呼んでいました。
米国のJackson Laboratoryという遺伝研究を行う会社に勤めていたColemanさんは、1965年に実験用のネズミ(マウス)の中にぶくぶくと太ったマウスの家系を発見しました。さまざまな症状が白人の糖尿病患者さんと似ていたことから、糖尿病マウスと呼びました。別のグループの研究で、視床下部が食欲を調節するセンターであることや、食欲には血液を流れる「何か」が大事であることが知られていました。
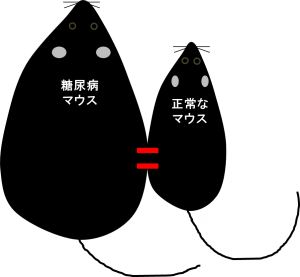
Colemanさんはこの「何か」が糖尿病マウスでも関係しているのではないかと考え、1969年に外科的に糖尿病マウスと普通のマウスの血管を繋ぐ実験をしました。この方法では2匹のマウスの血液がお互いの体を流れるので、血液中に「何か」があれば、どちらかのマウスに何かしらの影響が出ると考えられます。Colemanさんは糖尿病マウスの症状が良くなるかどうかを調べようとしたのですが、予想外なことに普通のマウスは食べるのをやめてしまい、やせ細って死んでしまいました。
他にも、糖尿病の症状は出さないけれども太っていて、何らかの機能異常が見られるマウスがいました。これを肥満マウスと呼び、同じように普通のマウスと血管を繋げました。すると今度は、肥満マウスは痩せていき、健康的な体になることができました。
最後に、糖尿病マウスと肥満マウスの血管を繋げると、肥満マウスは食べるのをやめてしまい、やせ細って死んでしまいました。
Colemanさんは、糖尿病マウスは満腹因子を作りすぎてしまっており、肥満マウスは満腹因子を作れないと推測しました。Colemanさんは満腹因子をつきとめたかったのですが、当時の生物学はそこまで発展していませんでした。
レプチンはどのように働くのか?
1986年、Friedmanさんは「分子がマウスの行動を左右する」という事実に興味を抱いたそうです。……ってなんのことだかわからないですよね。ここで言う「分子」とは、満腹因子のことです。満腹因子を作り出す遺伝子がおかしくなっていることでマウスの行動(ここで言う太ること)が変わることが面白かったのですね。そこで、Friedmanさんは満腹因子のDNA配列を突き止めることにしました。遺伝学はまだそれほど進んではいませんでしたが、満腹因子がマウスの6番染色体上にあることはわかっていました。そこでFriedmanさんはこの範囲を狭くしていくことにしました。
1994年までに、研究チームは約1000匹のマウスを用いて何百もの分子マーカーを使い、ついにDNA配列をつきとめました。さらに、抗原抗体反応を使って脂肪細胞から血中に分泌され、脳で働くことを明らかにしました。Friedmanさんはこのとき、満腹因子が動物をスリムにすることからギリシャ語の「痩せている」という意味のレプトスにちなんで「レプチン」と名付けました。
そして、1995年に脳の中の視床下部に働きかけることを発見しました。さらに糖尿病マウスでは、視床下部にあるレプチンがくっつく場所(レプチン受容体)に異常があり、視床下部で働きかけられないので、レプチンが血液内にたくさん余ってしまい、太っていることを発見しました。
実際の医療現場では
実際に、人間でも生まれつきレプチンをうまく作れない人がいます。その人は赤ちゃんのときから異常なほどに太っていたのですが、レプチン療法を行うことでスリムになりました。
食欲を抑えるのはレプチン。では食欲を出すのは…?
さて、レプチンは食欲を抑えるホルモンでしたが、反対に食欲を出すホルモンもあります。これを「オレキシン」といいます。オレキシンは柳沢正史先生(テキサス大学)が発見したホルモンで、視床下部から分泌されて脳に「おなかが減ったからご飯を食べようよ!」という命令を出します。こんな風に、私たちの食欲は主にレプチンとオレキシンで管理されています。
まとめ
レプチンの研究は生物学の発展(この研究には外科学・遺伝学・免疫学などたくさんの生物学が詰まっています)とともに進んできました。そして、新たな肥満学という分野を開きました。その成果によって、ColemanさんとFriedmanさんは2010年にノーベル賞の前哨戦とも言われるアルバート・ラスカー基礎医学研究賞を受賞し、毎年、ノーベル賞受賞者の予想を立てているトムソン・ロイターにもノミネートされています。
今年はこの二人なのではないかな、と私は予想しています。
その他の注目研究
そして…レプチンの研究以外では、新しい研究のやり方に注目しています。それは「光遺伝学(optogenetics)」です! この技術によって、脳でそれぞれの神経細胞がどんな働きをしているのかを細かく調べられるようになったのです。2006年にKarl Deisserothさん(写真 下)の研究グループが発表した方法です。
まず、神経細胞のスイッチをオンオフするような遺伝子(チャネルロドプシン・ハロロドプシン)をマウスに導入します。そしてマウスの脳内に光ファイバーを入れ、すごく狭い範囲に光を当てると少数の神経細胞だけを活動させることができます。顕微鏡の発展もあって、今までの方法では難しかった生きた状態で狭い範囲の神経細胞の働き方が見えてくることが期待されています。2012年に神経科学の基礎研究のきわめて優れた業績に対して贈られるチューリッヒ賞を受賞しました。

ノーベル生理学医学の発表は10月8日(月)日本時間の18時30分から。
お楽しみに!
<リンク>
2012年ノーベル生理学医学賞! テーマは「リプログラミング」(リンクは削除されました)







