お待たせしました!ノーベル化学チームからも、今年の受賞に関するお話です!
2020年ノーベル化学賞は、エマニュエル・シャルパンティエ博士とジェニファー・ダウドナ博士に贈られました。

テーマは「"for the development of a method for genome editing."(ゲノム編集方法の開発)」
ゲノム編集ってきいたことあるけど、どこがすごいのだろう‥‥という方も多いはず。
かくいう私もそのひとりでした。今日は一緒に2020年ノーベル化学賞をひもといていきましょう!
1953年、ワトソンとクリックはDNAの分子構造を報告しました。
今回の受賞内容を説明する文章のはじめに書かれていた文章です。
今回ノーベル化学賞を受賞したゲノム編集という技術が登場するには、まず生き物がいきていくための仕組みを理解する必要がありました。
そこで重要となる分子がDNAです。
なんと大きな分子だ…とアントラセンという数ナノメートルサイズのとても小さな分子を扱っていた竹腰は思いました。総合司会の綾塚が書いた事前記事参照!
https://blog.miraikan.jst.go.jp/articles/20201007post-379.html
この記事の前半では、まずはDNAを中心とした生き物のしくみをご紹介します。DNAのことはもう知っているよ!という方は、スクロールをして「ゲノム編集とは……」までお進みください。
DNAのすごみ
DNAは生き物のからだの中にあるのですが、実際にはとても小さな空間に折りたたまれておさまっています。
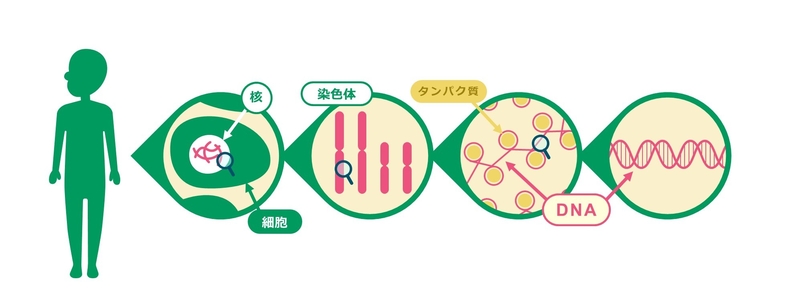
図:科学コミュニケーター三澤作成
DNAは生き物の種類によって異なり、同じ人間でも私の細胞とあなたの細胞では少しずつ異なるDNAをもっています。
ですが、私のなかの約37兆個の細胞はすべて同じDNAをもっています。同じように、あなたの細胞もすべてのあなたオリジナルのDNAをもっています(※1)。
(1970年代にこの事実を実験で証明したジョン・ガードン博士は2012年に生理学医学賞を受賞しています。)
この事実は本当にすごいことで、細胞が分裂し増えていく際に、同じようにDNAも”おおよそ間違いなく”コピーされるため、すべての細胞が同じDNAを維持できるのです。
※1 厳密には37兆個の細胞のすべてがまったく同じDNAというわけではありません。放射線が当たったり、後述するDNAを複製するときのミスで、少し変わってしまうことがあります。そうした変化が、がんの原因になることもあります。
そして、このDNAの構造がはしごのように連なった二重らせんになっていることを突き止めたのが、ワトソン博士とクリック博士です。きいたことある方もいるでしょうか?
(DNAの構造を解明したことで1962年にノーベル生理学医学賞を受賞しています。)
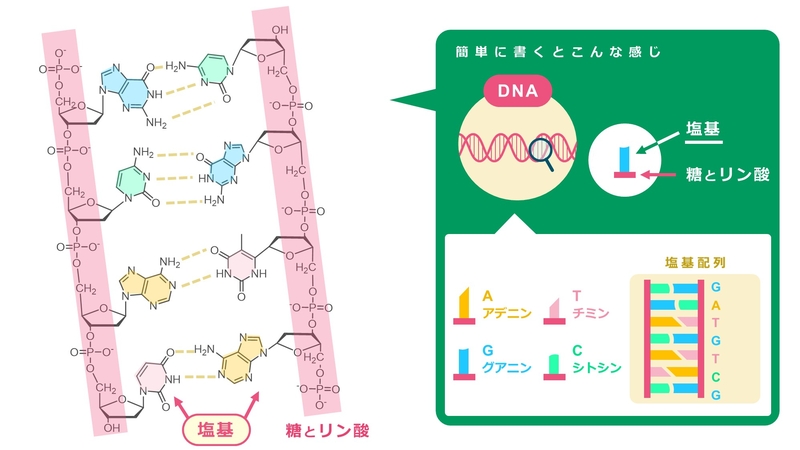
DNAをさらに詳しくみてみると、糖とリン酸という物質からできたひもに、アデニン:A、チミン:T、グアニン:G、シトシン:Cという4種類の塩基がぶらさがった構造になっていることも分かりました。
(やっと私でも想像できるサイズの分子の大きさになりました…)
生体のなかでのDNAは、AとT、GとCがそれぞれ対をつくるため、はしごのような構造をつくり、さらにそれがねじれています。「二重らせん構造」と呼んでいます。
DNAからタンパク質へ
では、次にこのDNAがからだのなかでどのように使われているかをみていきましょう。
DNAが使われるときには、DNAの塩基配列をもとにしてRNAという物質がつくられます。RNAはDNAをコピーしたような構造ですが、1本の鎖になります。さらにRNAの塩基配列をもとにタンパク質がつくられます。
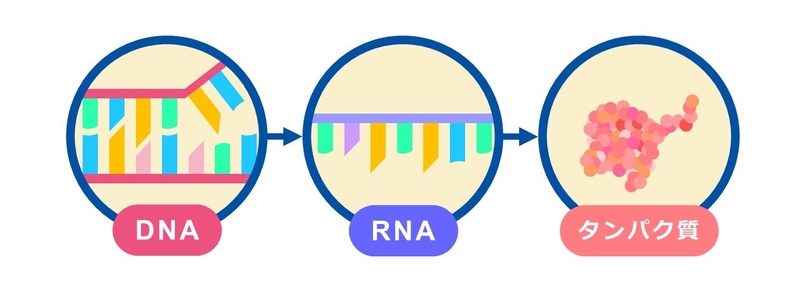
タンパク質は、からだの中で様々な役割を果たしています。例えば、筋肉を動かしたり、情報を伝えたり、糖分などの栄養や酸素を運んだり、病原体が入ってきたらやっつけたり、…タンパク質がないと私たちはやっていけません!
人間でいうとその数なんと10万種類!
この体のはたらきを担うタンパク質の設計図を書いているのがDNAの塩基配列なので、 “DNAはからだの設計図”とよばれているのです。
さて、ではいったいどうやって10万種類ものタンパク質をたった4種類の塩基配列からつくっているのでしょうか?
答えは簡単、組み合わせをつかうのです。
A, T, G, Cのうちから3つの塩基を選んで並べます。この3つの並びを一つの単位として、どのアミノ酸が使われるか決めています。
実は、タンパク質はこの20種類のアミノ酸が非常に長く連なったものです。
つまり、DNA上にA, T, G, Cをどのように並べるかで、最終的にどんなタンパク質ができるかが決まります。
さて、ここで本来 G A G という並びの部分が、G T G という並びになっていたとしましょう。そのDNAの配列からはグルタミン酸が使われるはずでしたが、かわりにバリンというアミノ酸が使われます。その場合、本来つくられるはずのタンパク質とは少し違うものができてしまいます。
これは実際に、赤血球のなかのヘモグロビンβというタンパク質に起きる変異で、この変異があると赤血球の酸素を運ぶ能力を著しく低下させます。鎌状赤血球症という病気の原因はこの変異です。
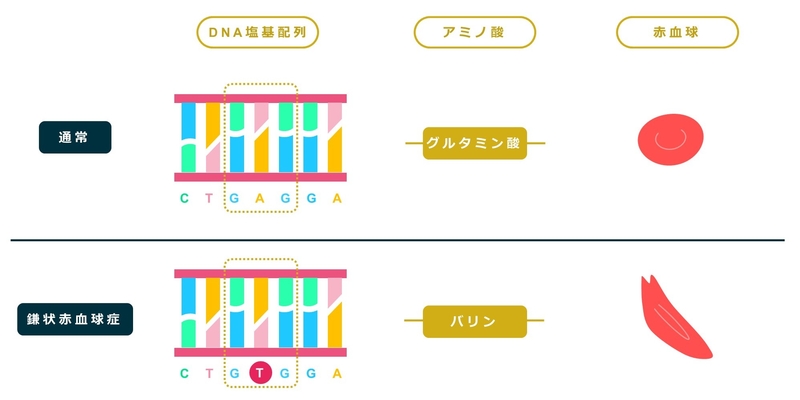
このようにたった1塩基の違いが生命現象に大きく影響を及ぼすことが分かります。
ここまでの遺伝子をめぐるお話をさらに詳しく知りたいという方は、こちらのトークもご覧ください。
以下のゲノム編集のお話にも深みが増すと思います。
「遺伝子をめぐる終わらない旅」
https://www.youtube.com/watch?v=VZJ2_uSKMRE&feature=emb_rel_pause
ゲノム編集とは……
さて、ここでやっとゲノム編集の話に戻りましょう。
ゲノム(全遺伝情報)は、さきほど紹介したDNAという物質に記録されています。
ゲノムを編集するということは、DNA上の塩基配列A, T, G, Cの一部を削除したり、新しいものを挿入したり、置き換えたりすることを意味しています。
例えば、塩基配列の一部が削除されると、目的のタンパク質がつくられなくなります。あえて特定のタンパク質をつくらせないことで、その遺伝子のはたらきを調べる基礎研究などに使われます。また、ジャガイモの毒となる成分をつくらせないなどの農業分野における応用例もあります。
新しい塩基配列を挿入することもでも、同じように特定のタンパク質をつくらないようにすることができます。また、がん細胞にのみ蛍光タンパク質をつくらせるように塩基配列を挿入し、特定の細胞の働きを追跡することもできます。
一塩基を置き換えることができれば、先ほどの鎌状赤血球症のような一部の塩基が変異してしまうことで起きる病気などの治療への応用も期待されます。
このように、ゲノムを書き換えることで、生き物のなかではたらくタンパク質などの機能を加えたり、なくしたりすることができます。
CRISPR-Cas9を用いたゲノム編集
そして、今回紹介するゲノム編集で使うのは、CRISPR-Cas9(クリスパー・キャスナイン)と呼ばれるツールです。
20個ほどの塩基配列からなるRNA(ガイドRNAとよびます)とCas9という酵素(タンパク質分子)からなっています。研究者は、編集したいと思う遺伝子の配列に合わせてガイドRNAを作成します。通常、遺伝子は非常にたくさんの塩基配列からなりますが、その中から20個程度の配列に合うようにガイドRNAをつくります。
実際に編集する際には、まず目的となるDNAの塩基配列をガイドRNAが認識します。この特定の配列を認識するというのが、「ゲノム編集」技術のカギといってよいでしょう。認識した配列にくっつき、そこでDNAを切断します。
細胞にしてみれば、からだの設計図であるDNAを切断されてしまう訳ですから一大事です。でも、実は自然でも、放射線などにあたるとこうした切断が実際に起きることがあり、そのような切断が生じたときには、細胞にはそれを「修復」してつなぎあわせる仕組みが備わっています。
そして、その細胞がもともともつ「修復」の仕組みは、ミスをすることがあります。その結果、一定の確率で塩基配列A, T, G, Cの一部が欠けたり、逆に本来はなかったものが挿入されることがあります。また、切断した箇所とよく似た塩基配列の断片をCRISPR-Cas9と一緒に加えておくと“間違えて”その断片を使って修復が行われることがあります。欠損や挿入に比べると、頻度は低くなりますが、自分が変えたい配列にすることもできるのです。
さきほど、DNAは”おおよそ間違いなく” コピーされるといいましたが、もしコピーし間違えてしまった場合にも、この修復の機能がはたらき、間違えた部分のDNAを切り取ったり、くっつけなおしたりする修復のしくみが備わっているのです。
詳しくは、2015年ノーベル化学賞受賞研究「DNA修復のメカニズムの解明」についての科学コミュニケーターブログも読んでみてください
https://blog.miraikan.jst.go.jp/articles/201510072015dna-1.html
細胞にもとから備わっている修復という仕組みを利用しつつ、塩基配列の改変を行う技術が今回のゲノム編集です。
ゲノム編集ツールCRISPR-Cas9のしくみ
図を使いながら、シャルパンティエ博士とダウドナ博士が作ったCRISPR-Cas9という道具が具体的にどのように働いているのかを説明しましょう。
1.編集したいDNAをもつ細胞に、あらかじめ用意したガイドRNAと、Cas9というタンパク質をいれます。すると、ガイドRNA がCas9に結合し、Cas9の構造が大きく変わります。つまり、DNAまってるぜ!という待機状態です。
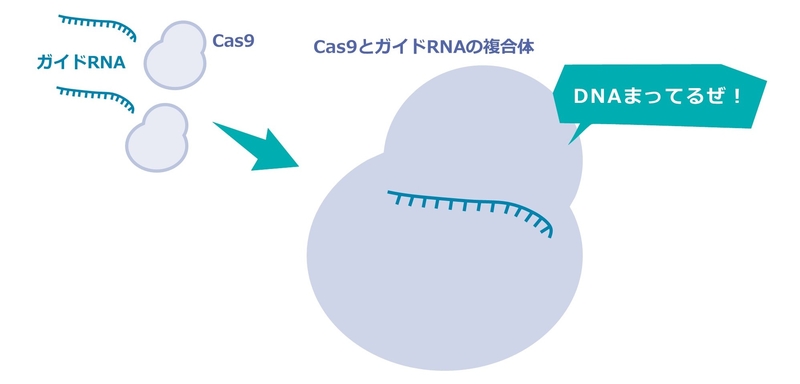
2.そこにDNAがはいっていきます。その際、DNA上に「PAM」と呼ばれる塩基の数にして3個ほどの特定の配列があると、DNAのはしごがほどけて、かわりにガイドRNAの一部分がくっつきます。
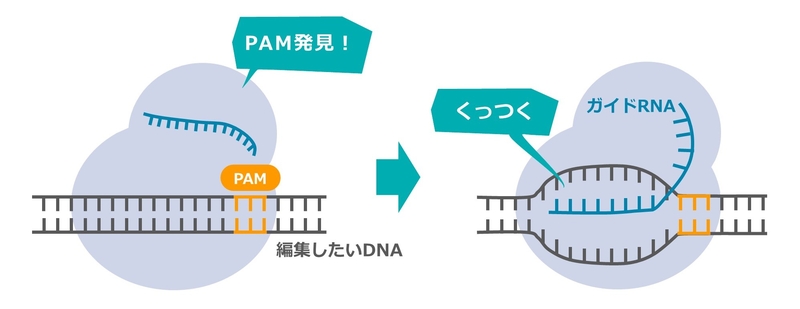
3.ガイドRNAとターゲットとするDNAが一致した場合、Cas9がDNAのねらった部分を切ります
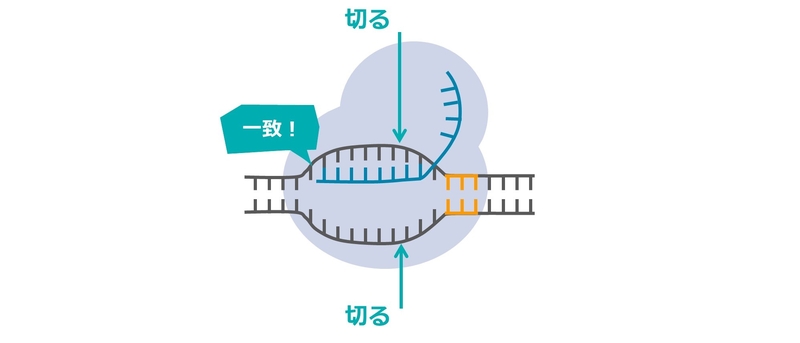
4.その後、DNAを修復する仕組みがはたらきます。もとあったDNA配列の機能をなくしたい場合はこのままですが、新しい配列を挿入したい場合はその配列の断片を加えておきます。
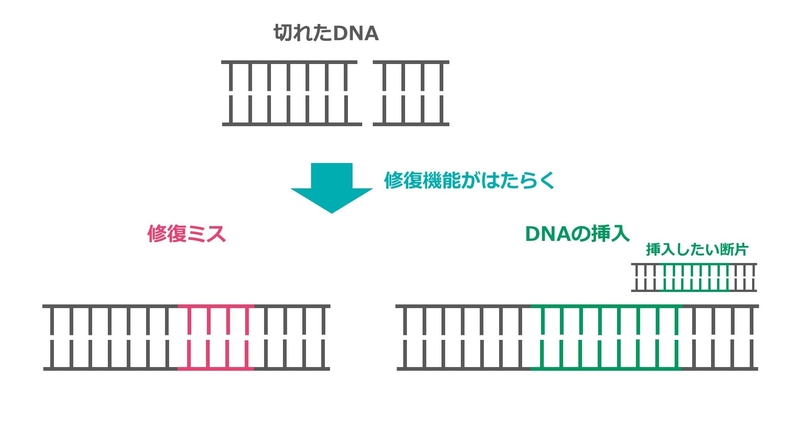
意図的にゲノムの狙った部分を切ることができる、それがCRISPR-Cas9というゲノム編集ツールです。
自分が編集したい塩基配列に合わせてガイドRNAをつくれば、PAM配列が近くにあれば原理的にDNAのどの場所でも編集することができます。
CRISPR-Cas9の威力
実はCRISPR-Cas9登場以前から、DNAを編集する方法はありました。ですが、先行するほかのゲノム編集ツールとは異なり、この方法は、特定のDNA配列を認識するツールとしてガイドRNAを使っています。これは比較的に簡単に安く作れるため、準備期間、コストなどの点からCRISPR-Cas9は圧倒的に使いやすかったのです。2012年に発表されるやいなや、瞬く間に世界中の研究者が使うようになりました。
さらに、初めの方にお伝えした、DNAが4種類の塩基からできていて、その並び方をもとにタンパク質がつくられる、というのはどの生き物ももっているしくみなので、このCRISPR-Cas9という方法がいろんな生き物に適用できるという点も素晴らしい点です。
生命科学の研究ではマウスなど特定の動物がよく研究に使われていました。マウスでは例外的に特定の遺伝子を働かなくする技術がすでにあり、それは2007年のノーベル生理学医学賞の対象となるような素晴らしい成果でした。ですが、ほとんどの種類の生き物は同じ手法が使えません。
CRISPR-Cas9は、ごく一部の生き物に限られていた研究手法をほとんどの種類の生き物にも可能にしたのです(マウスでもCRISPR-Cas9を使う方が先行技術よりも安く時間もかからないため、現在ではゲノム編集の方がよく使われています)。
もとはといえば……
この技術、もともとはゲノムを編集するために研究されていたわけではない、という点もポイントです。
実は、シャルパンティエ博士はもともと微生物学の専門家で化膿レンサ球菌という細菌を研究していました。この細菌がウイルスから自分を守るために使っていた免疫のシステムを詳しく調べるところからこの研究はスタートしました。そして、RNAを研究していたダウドナ博士と一緒に今回のシステムを研究するに至ったのです。
もともと細菌という生き物がもっていたタンパク質が、別の生き物のDNAを切ると考えると面白いですよね。
技術のもととなった細菌の免疫システムについて詳しく知りたい方はこちらの科学コミュニケーターブログもお読みください。
https://blog.miraikan.jst.go.jp/articles/201509242015crisprcas9.html
「人類の幸福に貢献する研究」に与えられるノーベル賞
ゲノムDNAからタンパク質をつくるという生き物のしくみを理解し、さらに細菌が自分を守るしくみを理解することで生まれたゲノム編集の技術。
長い歴史を重ねながらそのしくみを理解してきたことで、私たちは今それを操作する方法を手にいれました。
「このツールには巨大な力があり、私たち皆に影響を与えます。それは基礎科学に革命をもたらしただけでなく、革新的な作物を生み出し、画期的な新しい医療をもたらすでしょう。」とノーベル化学委員会の委員長Claes Gustafsson氏は述べています。
一方で、ノーベル賞の発表資料にはこんなふうにも書かれていました。
「このような技術がもつ恩恵に加えて、この技術が誤用される可能性もあります。」
遺伝子の一部を編集することができるこの技術は、上記に述べた鎌状赤血球症など遺伝性疾患の治療への応用などが期待されています。
一方で、受精卵などに施せば、その世代だけでなく、その子や孫の世代にも影響を及ぼす可能性があります。このような使い方に関しては、現在、国際的にも議論されています。
さらに、目的以外の変異が入ってしまう可能性など、安全性の向上の余地もまだまだ残されているようです。
いきものの“もと”ともいえるゲノムを編集することができる、この新しい技術が生命科学の分野を新たなステージにおしあげ、そして加速させていることは間違いありません。さらに、近い将来その影響は私たちのそばにもやってくるはずです。
人類の幸福に貢献する研究に贈られるノーベル賞、この研究を真に人々に幸福をもたらすものとして扱っていけるのかどうか、問われているのかもしれません。
編集後記
発表直前に公開された綾塚のブログで、「分子が世界を変えるんだ!」と言っていたところ、まさに塩基という小さな分子が、いきもののしくみという大きな世界を変えてしまうような研究の受賞でした。その世界観をすこしでも味わっていただけたでしょうか…?
世界変えすぎだよ!と目の前がぐるぐるしそうですが、まさに発展中の研究を今後も見守っていきたいと思います。
エマニュエル・シャルパンティエ博士、ジェニファー・ダウドナ博士、おめでとうございました!







